9 0 5 7 8
论文已发表
注册即可获取德孚的最新动态
IF 收录期刊
- 2.6 Breast Cancer (Dove Med Press)
- 3.9 Clin Epidemiol
- 3.3 Cancer Manag Res
- 3.9 Infect Drug Resist
- 3.6 Clin Interv Aging
- 4.8 Drug Des Dev Ther
- 2.8 Int J Chronic Obstr
- 8.0 Int J Nanomed
- 2.3 Int J Women's Health
- 3.2 Neuropsych Dis Treat
- 4.0 OncoTargets Ther
- 2.2 Patient Prefer Adher
- 2.8 Ther Clin Risk Manag
- 2.7 J Pain Res
- 3.3 Diabet Metab Synd Ob
- 4.3 Psychol Res Behav Ma
- 3.4 Nat Sci Sleep
- 1.9 Pharmgenomics Pers Med
- 3.5 Risk Manag Healthc Policy
- 4.5 J Inflamm Res
- 2.3 Int J Gen Med
- 4.1 J Hepatocell Carcinoma
- 3.2 J Asthma Allergy
- 2.3 Clin Cosmet Investig Dermatol
- 3.3 J Multidiscip Healthc

中国在 ChiCTR 和 ClinicalTrials.gov 平台注册的 COVID-19 临床试验的特征分析
Authors Huang J, He Y, Su Q, Yang J
Received 17 March 2020
Accepted for publication 16 May 2020
Published 29 May 2020 Volume 2020:14 Pages 2159—2164
DOI https://doi.org/10.2147/DDDT.S254354
Checked for plagiarism Yes
Review by Single-blind
Peer reviewer comments 5
Editor who approved publication: Dr Tuo Deng
目的:评价中国注册的新型冠状病毒肺炎 (COVID-19) 临床试验的基本特征。
方法:通过 ChiCTR 和 ClinicalTrials.gov 数据库检索中国注册的 COVID-19 临床试验,评价其研究设计、样本量、主要研究指标和干预措施。
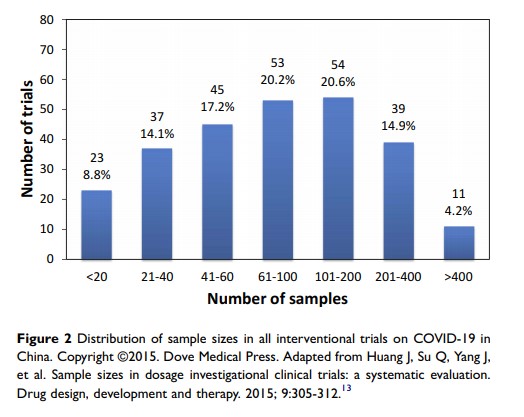
结果:截止 2020 年 3 月 10 日,共检索到 262 项干预性临床试验。 在 262 项试验中,181 项占 69.1% 的试验为两组试验,200 项占 76.3% 的试验为随机平行对照试验,24 项为双盲试验仅占 9.2%,60.3% 的试验样本量在 100 例以内(包括 100)。 60 项占 22.9% 的试验将症状改善作为主要指标,43 项占 16.4% 的试验将病毒阴转率或阴转时间作为主要指标。 在 262 项干预研究中,有 105 项占 40.1% 为化学药物和生物制品试验,抗病毒药物占 15.3% ,疟疾药物占 8.4%。 在所有试验中,27.9% 的研究为中药干预试验,10.3% 的研究为细胞治疗试验,5.0% 的研究为血浆治疗试验。
结论:本研究分析了中国注册的 COVID-19 临床试验的情况,为 COVID-19 的治疗和预防提供了临床试验设计的基本特征,也为其他国家将要开展的抗 COVID-19 临床试验提供有用的信息。
关键词:新型冠状病毒肺炎,临床试验,干预措施,随机,盲法